دوره 13، شماره 5 - ( شماره ویژه 1398 )
جلد 13 شماره 5 صفحات 675-666 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Hejazi S M, Haghgoo H A, Karbalaei Nouri A, Biglarian A, Akbarfahimi N. The Relationship Between Memory Impairment and Health Indicators of the Elderly With Parkinson Disease. Salmand: Iranian Journal of Ageing 2019; 13 (5) :666-675
URL: http://salmandj.uswr.ac.ir/article-1-1576-fa.html
URL: http://salmandj.uswr.ac.ir/article-1-1576-fa.html
حجازی سیده مطهره، حقگو حجت اله، کربلایی نوری اشرف، بیگلریان اکبر، اکبر فهیمی نازیلا. ارتباط بین اختلال حافظه (بینایی و کلامی) با شاخصهای سلامت سالمندان دارای پارکینسون. سالمند: مجله سالمندی ایران. 1398; 13 (5) :666-675
1- گروه کاردرمانی، دانشگاه علوم بهزیستی و توانبخشی، تهران، ایران.
2- گروه آمار زیستی، مرکز تحقیقات عوامل اجتماعی مؤثر بر سلامت، دانشگاه علوم بهزیستی و توانبخشی، تهران، ایران. ،nouri.uswr@gmail.com
3- گروه آمار زیستی، مرکز تحقیقات عوامل اجتماعی مؤثر بر سلامت، دانشگاه علوم بهزیستی و توانبخشی، تهران، ایران.
2- گروه آمار زیستی، مرکز تحقیقات عوامل اجتماعی مؤثر بر سلامت، دانشگاه علوم بهزیستی و توانبخشی، تهران، ایران. ،
3- گروه آمار زیستی، مرکز تحقیقات عوامل اجتماعی مؤثر بر سلامت، دانشگاه علوم بهزیستی و توانبخشی، تهران، ایران.
متن کامل [PDF 2258 kb]
(3023 دریافت)
| چکیده (HTML) (18975 مشاهده)
متن کامل: (5065 مشاهده)
مقدمه
طبق گزارش سازمان جهانی بهداشت، تعداد سالمندان جهان تا سال 2050 به دو میلیارد نفر خواهد رسید و از هر پنج نفر، یک نفر سالمند خواهد بود [1]. از آنجا که تعداد سالمندان بهسرعت در حال افزایش است، توجه به سلامت آنان اهمیت ویژهای دارد [2]. پارکینسون از جمله بیماریهای مغز و اعصاب مزمن و پیشرونده است که بعد از آلزایمر، شایعترین بیماری مخرب اعصاب به حساب میآید [3]. شیوع پارکینسون در سنین بین 50 تا 70سالگی بیشتر است [3] و بعد از 60سالگی میزان بروز این بیماری به صورت چشمگیری افزایش مییابد. سالمندی یکی از برههای خطرناک برای ابتلا به پارکینسون است؛ به نحوی که میزان احتمال بروز پارکینسون بین 45 تا 55سالگی، 02/0 درصد است که تا 85سالگی به 77/8 درصد میرسد [4].
مشخصه این بیماری سفتی عضلانی پیشرونده تدریجی، لرزش و ازدسترفتن مهارتهای حرکتی است [5 ،3]. بیماری پارکینسون فقط به مشکلات حرکتی ختم نمیشود، بلکه دامنه وسیعی از نقایص شناختی، مشکلات اتونوم و اختلالات خواب را هم در پی دارد و به افزایش ناتوانی و کاهش کیفیت زندگی منجر میشود [6]. حدود یکسوم افراد مبتلا به پارکینسون، مشکلات شناختی عمده دارند که اغلب پس از 4 سال دو برابر میشود [7]. شایعترین مشکلات شناختی در این افراد دمانس است که میزان شیوعش 40 درصد است و این میزان بعد از گذشت 8 سال از بیماری، به 78 درصد میرسد که دو تا شش برابر جامعه معمولی است [8]. علاوه بر این، افراد مبتلا به پارکینسون مشکلاتی در زمینه عملکرد اجرایی، توجه، روابط فضایی و حافظه نیز دارند که نسبت به دمانس شیوع نسبتاً کمتری دارد [8]. همچنین مطالعات نشان میدهد وجود یکسری از اختلالات و بیماریها مثل اختلال در خواب یا اختلال در تنظیم فشار خون ممکن است فرد را برای ابتلا به نواقص شناختی مثل اختلال در حافظه، توجه، عملکرد اجرایی و حافظه دیداریفضایی مستعدتر کند [12-9].
در مطالعهای که برای بررسی ارتباط بین اختلال خواب و ابتلا به اختلال شناختی در سالمندان مبتلا به پارکینسون انجام شد، بیان شد ابتلا به اختلال خواب و آپنه انسدادی خواب میتواند باعث بروز علائم غیرحرکتی در این افراد شود [11]. همچنین در بررسی ارتباط بین اختلالات شناختی و اختلال فشار خون در سالمندان مبتلا به پارکینسون ، بیان شد که 53 درصد سالمندان مبتلا به پارکینسون دچار افت فشار خون و وضعیتی میشوند که روی شدت نواقص شناختی آنان تأثیر میگذارد [9].
با توجه به مطالب بیانشده میتوان گفت برخی شاخصهای سلامت مثل فشار خون طبیعی، خواب خوب در سالمندان مبتلا به پارکینسون دچار اختلال میشود. بنابراین، بررسی ارتباط بین شاخصهای سلامت و اختلالات شناختی میتواند به این بیماران کمک کند و شاید ارتباطی میان این شاخصها با بروز نقایص شناختی مثل حافظه در این افراد وجود داشته باشد، اما ارتباط دقیقی بین عوامل پیشگفته با شیوع و بروز مشکلات حافظه مشخص نشده است [10 ،9]. از طرفی با توجه به شیوع اختلال شناختی در این افراد، ارزیابی جامع و دقیق در حوزه کاردرمانی و سایر حوزههای توانبخشی شناختی برای تشخیص بهموقع و درمان این علائم برای بیمار و خانواده او میتواند بسیار کمککننده باشد. بدین منظور، در این مطالعه ارتباط بین شاخصهای سلامت و اختلالات شناختی در این بیماران بررسی شد.
روش مطالعه
این مطالعه از نوع مطالعات توصیفیمقطعی همبستگی بود. جامعه آماری مطالعه شامل تمام سالمندان مبتلا به پارکینسون بین 60 تا 70ساله در شهر تهران و نمونه موردمطالعه سالمندان مبتلا به پارکینسون مراجعهکننده به بیمارستانهای شهر تهران بود که به صورت دردسترس انتخاب شدند. حجم نمونه مطالعهشده با درنظرگیری توان آزمون، 80 درصد و ضریب اطمینان 95 درصد، 25 نفر و با 20 درصد افزایش احتمال ریزش مراجعان، 30 نفر در نظر گرفته شد. پس از گرفتن مجوزهای لازم از مدیریت مراکز درمانی، نمونههای موردمطالعه، با معیارهای ورود، شامل سن بین 60 تا 70 سال، مدت زمان ابتلا بین یک تا 6 سال، توانایی خواندن و نوشتن، توانایی برقراری ارتباطات کلامی و پیروی از دستورات، نبود آفازی و مشکلات زبان و معیارهای خروج شامل نبود روند صحیح پاسخگویی به سؤالات و پرسشنامه و تمایلنداشتن به همکاری مراجعان در هر مرحله از پژوهش، انتخاب شدند.
پس از کسب رضایت آگاهانه از شرکتکنندگان، فرایند جمعآوری اطلاعات آغاز شد. در ابتدا از آزمون مونترال برای غربالگری اختلالات شناختی استفاده شد و برای تعیین اختلال حافظه کلامی از آزمون وکسلر (حافظه بزرگسال) و برای بررسی حافظه بینایی از آزمون آندره ری استفاده شد. همچنین برای بررسی اختلال خواب، پرسشنامه کیفیت خواب پیتزبورگ استفاده شد. پس از تکمیل آزمونها، دادهها با نسخه 22 نرمافزار SPSS تجزیه و تحلیل شدند. برای جمعآوری دادهها از چهار آزمون استفاده شد که در ادامه توضیح داده میشوند.
آزمون شناختی مونترال
آزمون شناختی مونترال یک ابزار ساده، معتبر و حساس برای غربالگری اختلال شناختی است که در ایران برای افراد مبتلا به پارکینسون اعتبارسنجی شده است. امساکی و همکاران در سال 2012 هنجاریابی و بررسی ویژگیهای روانسنجی آزمون ارزیابی شناختی مونترال در افراد مبتلا به پارکینسون در ایران را انجام دادند که ضریب آلفای کرونباخ 77 درصد و روایی همزمان 79/0 درصد برای آن تعیین شد. این آزمون پایایی آزمونبازآزمون و ثبات درونی بالایی خوب و نمرات آن با نمرات سایر مقیاسهای نوروسایکولوژیک همبستگی بالایی دارد. این مقیاس تکالیف سختی در زمینه عملکرد اجرایی، تواناییهای زبانی سطح بالاتر، حافظه و پردازش دیداریفضایی پیچیده دارد. در فرم اصلی مقیاس نمره کل، 30 است، اما نمره 26 و بیشتر عادی تلقی میشود [13].
آزمون حافظه وکسلر بزرگسالان
آزمون حافظه وکسلر بزرگسالان برای ارزیابی حافظه شرکتکنندگان است. این آزمون خردهآزمونهای کلامی شامل اطلاعات عمومی، ادراک کلامی، حافظه عددی به صورت مستقیم و معکوس، استدلال ریاضی، تشابهات و لغات تکمیلی دارد. خردهآزمونهای غیرکلامی شامل تصاویر ناقص، ادراک تصویری، استدلال علمی، ساختن تصاویر و دقت و تداعی است.
امید ساعد و همکاران این آزمون را در سال 2009 اعتبارسنجی کردند که ضریب پایایی آن بالای 0/8و ضریب همبستگی اعتبار آن بین 0/8 و 0/4 گزارش شده است [14].
آزمون آندره ری
آزمون آندره ری برای بررسی ادراک و حافظه بینایی است، که متشکل از دو کارت A و B است که هریک به طور مجزا و به مناسبت، انتخاب و استفاده میشوند. کارت A متشکل از 18 جزء ادراکی است. کارت B از 11 جزء هندسی تشکیل شده و مکمل کارت A است. در ابتدا از آزمودنی خواسته میشود به دلخواه تصویر یکی از کارتها را بکشد بعد از اتمام کار و پس از گذشت 3 دقیقه از او خواسته میشود دوباره تصویر را بکشد. مرحله نخست ترسیم به حساب توان رشد ترسیمی و ساختیابی ادراکی و مرحله دوم، با توجه به کمیت و کیفیت ترسیم مرحله نخست، سطح کارکرد حافظه دیداری را نشان خواهد داد. در کارت B مجموع نمرات کسبشده، 29 و در کارت A مجموع نمرات 36 است. کارت B برای ارزیابی ادراک و حافظه بینایی کودکان و کارت A برای بزرگسالان است. در این مطالعه نتایج کارت A تحلیل و بررسی شد. این آزمون را پناهی در سال 2005 در ایران اعتبارسنجی کرد و ضریب روایی آن حدود 50 و ضریب پایایی حدود 59 برآورد شده است [15].
پرسشنامه مربوط به اختلالات خواب پیتزبورگ
این پرسشنامه برای تعیین کیفیت خواب است که در اصل 9 گویه دارد، اما چون سؤال پنج خود شامل 10 گویه فرعی است، بنابراین کل پرسشنامه 19 آیتم دارد که از صفر تا 3 نمرهگذاری میشود. این پرسشنامه مؤلفههای مدت زمان خواب، کیفیت ذهنی خواب، تأخیر در بهخوابرفتن، میزان بازدهی خواب، اختلالات خواب، استفاده از داروهای خوابآور و اختلالات عملکردی روزانه را ارزیابی میکند. در این پرسشنامه کسب نمره کل بیشتر از 5 به معنی کیفیت خواب ضعیف است. شهریفر و حیدری این پرسشنامه را در سال 2011 در ایران اعتبارسنجی کردند و روایی 0/86 و پایایی 0/89 برای آن به دست آمد. ضریب الفای کرونباخ این پرسشنامه 0/78 تا 0/82 گزارش شده است [17 ،16].
یافتهها
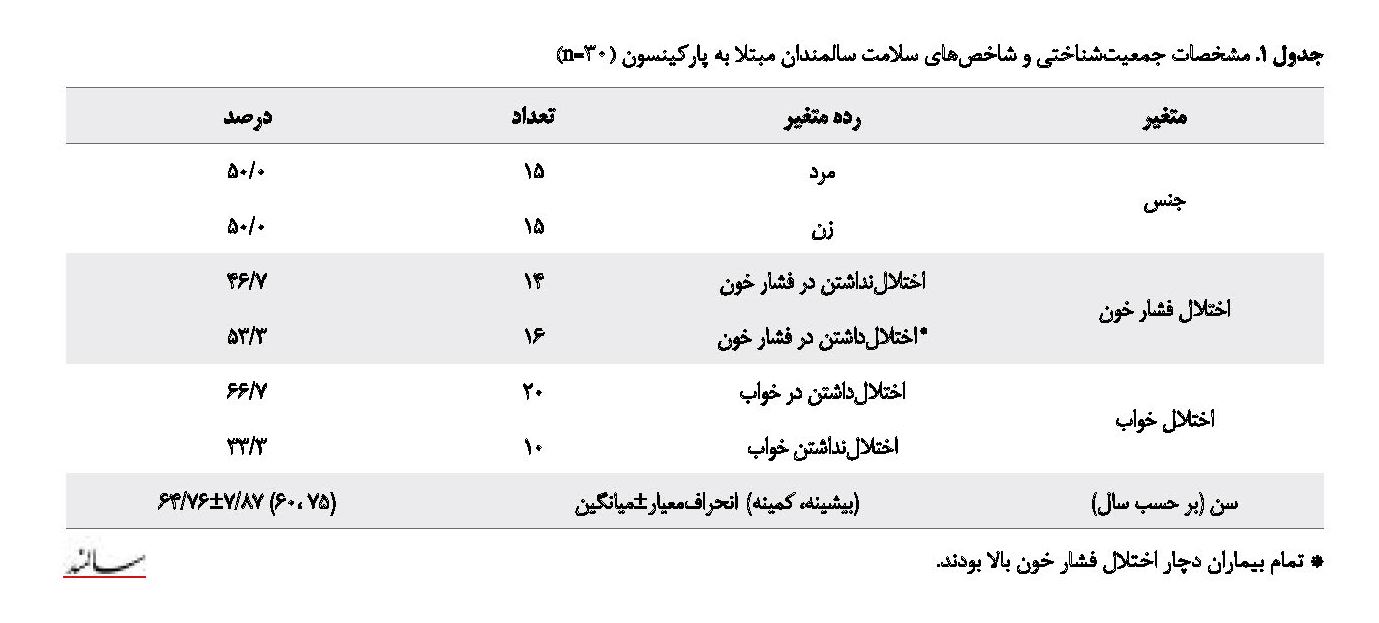
نتایج بهدستآمده از بررسی 30 نمونه شرکتکننده در این پژوهش نشان داد جنسیت افراد، مساوی (50 درصد بیماران مذکر و 50 درصد مؤنث) و میانگین سنیشان 76/64 بود. همچنین بیش از 50 درصد افراد فشار خون بالا و بیش از 60 درصد اختلال خواب داشتند که وضعیت متغیرهای اصلی در جدول شماره 1 نشان داده شده است. تمام متغیرها بر اساس آزمون شاپیروویلکز توزیع نرمال داشتند (P>0/05). در جدول شماره 2 وضعیت شناختی (حافظه کلامی و بینایی) سالمندان نشان داده شده است که بیش از 96 درصد از سالمندان در حافظه بینایی و 70 درصد در حافظه کلامی اختلال داشتند. همچنین برای بررسی ارتباط بین متغیرهای حافظه کلامی و بینایی با اختلالات فشار خون و خواب از ضریب همبستگی اسپیرمن استفاده شد که در جدول شماره 3 بررسی شده است.
طبق گزارش سازمان جهانی بهداشت، تعداد سالمندان جهان تا سال 2050 به دو میلیارد نفر خواهد رسید و از هر پنج نفر، یک نفر سالمند خواهد بود [1]. از آنجا که تعداد سالمندان بهسرعت در حال افزایش است، توجه به سلامت آنان اهمیت ویژهای دارد [2]. پارکینسون از جمله بیماریهای مغز و اعصاب مزمن و پیشرونده است که بعد از آلزایمر، شایعترین بیماری مخرب اعصاب به حساب میآید [3]. شیوع پارکینسون در سنین بین 50 تا 70سالگی بیشتر است [3] و بعد از 60سالگی میزان بروز این بیماری به صورت چشمگیری افزایش مییابد. سالمندی یکی از برههای خطرناک برای ابتلا به پارکینسون است؛ به نحوی که میزان احتمال بروز پارکینسون بین 45 تا 55سالگی، 02/0 درصد است که تا 85سالگی به 77/8 درصد میرسد [4].
مشخصه این بیماری سفتی عضلانی پیشرونده تدریجی، لرزش و ازدسترفتن مهارتهای حرکتی است [5 ،3]. بیماری پارکینسون فقط به مشکلات حرکتی ختم نمیشود، بلکه دامنه وسیعی از نقایص شناختی، مشکلات اتونوم و اختلالات خواب را هم در پی دارد و به افزایش ناتوانی و کاهش کیفیت زندگی منجر میشود [6]. حدود یکسوم افراد مبتلا به پارکینسون، مشکلات شناختی عمده دارند که اغلب پس از 4 سال دو برابر میشود [7]. شایعترین مشکلات شناختی در این افراد دمانس است که میزان شیوعش 40 درصد است و این میزان بعد از گذشت 8 سال از بیماری، به 78 درصد میرسد که دو تا شش برابر جامعه معمولی است [8]. علاوه بر این، افراد مبتلا به پارکینسون مشکلاتی در زمینه عملکرد اجرایی، توجه، روابط فضایی و حافظه نیز دارند که نسبت به دمانس شیوع نسبتاً کمتری دارد [8]. همچنین مطالعات نشان میدهد وجود یکسری از اختلالات و بیماریها مثل اختلال در خواب یا اختلال در تنظیم فشار خون ممکن است فرد را برای ابتلا به نواقص شناختی مثل اختلال در حافظه، توجه، عملکرد اجرایی و حافظه دیداریفضایی مستعدتر کند [12-9].
در مطالعهای که برای بررسی ارتباط بین اختلال خواب و ابتلا به اختلال شناختی در سالمندان مبتلا به پارکینسون انجام شد، بیان شد ابتلا به اختلال خواب و آپنه انسدادی خواب میتواند باعث بروز علائم غیرحرکتی در این افراد شود [11]. همچنین در بررسی ارتباط بین اختلالات شناختی و اختلال فشار خون در سالمندان مبتلا به پارکینسون ، بیان شد که 53 درصد سالمندان مبتلا به پارکینسون دچار افت فشار خون و وضعیتی میشوند که روی شدت نواقص شناختی آنان تأثیر میگذارد [9].
با توجه به مطالب بیانشده میتوان گفت برخی شاخصهای سلامت مثل فشار خون طبیعی، خواب خوب در سالمندان مبتلا به پارکینسون دچار اختلال میشود. بنابراین، بررسی ارتباط بین شاخصهای سلامت و اختلالات شناختی میتواند به این بیماران کمک کند و شاید ارتباطی میان این شاخصها با بروز نقایص شناختی مثل حافظه در این افراد وجود داشته باشد، اما ارتباط دقیقی بین عوامل پیشگفته با شیوع و بروز مشکلات حافظه مشخص نشده است [10 ،9]. از طرفی با توجه به شیوع اختلال شناختی در این افراد، ارزیابی جامع و دقیق در حوزه کاردرمانی و سایر حوزههای توانبخشی شناختی برای تشخیص بهموقع و درمان این علائم برای بیمار و خانواده او میتواند بسیار کمککننده باشد. بدین منظور، در این مطالعه ارتباط بین شاخصهای سلامت و اختلالات شناختی در این بیماران بررسی شد.
روش مطالعه
این مطالعه از نوع مطالعات توصیفیمقطعی همبستگی بود. جامعه آماری مطالعه شامل تمام سالمندان مبتلا به پارکینسون بین 60 تا 70ساله در شهر تهران و نمونه موردمطالعه سالمندان مبتلا به پارکینسون مراجعهکننده به بیمارستانهای شهر تهران بود که به صورت دردسترس انتخاب شدند. حجم نمونه مطالعهشده با درنظرگیری توان آزمون، 80 درصد و ضریب اطمینان 95 درصد، 25 نفر و با 20 درصد افزایش احتمال ریزش مراجعان، 30 نفر در نظر گرفته شد. پس از گرفتن مجوزهای لازم از مدیریت مراکز درمانی، نمونههای موردمطالعه، با معیارهای ورود، شامل سن بین 60 تا 70 سال، مدت زمان ابتلا بین یک تا 6 سال، توانایی خواندن و نوشتن، توانایی برقراری ارتباطات کلامی و پیروی از دستورات، نبود آفازی و مشکلات زبان و معیارهای خروج شامل نبود روند صحیح پاسخگویی به سؤالات و پرسشنامه و تمایلنداشتن به همکاری مراجعان در هر مرحله از پژوهش، انتخاب شدند.
پس از کسب رضایت آگاهانه از شرکتکنندگان، فرایند جمعآوری اطلاعات آغاز شد. در ابتدا از آزمون مونترال برای غربالگری اختلالات شناختی استفاده شد و برای تعیین اختلال حافظه کلامی از آزمون وکسلر (حافظه بزرگسال) و برای بررسی حافظه بینایی از آزمون آندره ری استفاده شد. همچنین برای بررسی اختلال خواب، پرسشنامه کیفیت خواب پیتزبورگ استفاده شد. پس از تکمیل آزمونها، دادهها با نسخه 22 نرمافزار SPSS تجزیه و تحلیل شدند. برای جمعآوری دادهها از چهار آزمون استفاده شد که در ادامه توضیح داده میشوند.
آزمون شناختی مونترال
آزمون شناختی مونترال یک ابزار ساده، معتبر و حساس برای غربالگری اختلال شناختی است که در ایران برای افراد مبتلا به پارکینسون اعتبارسنجی شده است. امساکی و همکاران در سال 2012 هنجاریابی و بررسی ویژگیهای روانسنجی آزمون ارزیابی شناختی مونترال در افراد مبتلا به پارکینسون در ایران را انجام دادند که ضریب آلفای کرونباخ 77 درصد و روایی همزمان 79/0 درصد برای آن تعیین شد. این آزمون پایایی آزمونبازآزمون و ثبات درونی بالایی خوب و نمرات آن با نمرات سایر مقیاسهای نوروسایکولوژیک همبستگی بالایی دارد. این مقیاس تکالیف سختی در زمینه عملکرد اجرایی، تواناییهای زبانی سطح بالاتر، حافظه و پردازش دیداریفضایی پیچیده دارد. در فرم اصلی مقیاس نمره کل، 30 است، اما نمره 26 و بیشتر عادی تلقی میشود [13].
آزمون حافظه وکسلر بزرگسالان
آزمون حافظه وکسلر بزرگسالان برای ارزیابی حافظه شرکتکنندگان است. این آزمون خردهآزمونهای کلامی شامل اطلاعات عمومی، ادراک کلامی، حافظه عددی به صورت مستقیم و معکوس، استدلال ریاضی، تشابهات و لغات تکمیلی دارد. خردهآزمونهای غیرکلامی شامل تصاویر ناقص، ادراک تصویری، استدلال علمی، ساختن تصاویر و دقت و تداعی است.
امید ساعد و همکاران این آزمون را در سال 2009 اعتبارسنجی کردند که ضریب پایایی آن بالای 0/8و ضریب همبستگی اعتبار آن بین 0/8 و 0/4 گزارش شده است [14].
آزمون آندره ری
آزمون آندره ری برای بررسی ادراک و حافظه بینایی است، که متشکل از دو کارت A و B است که هریک به طور مجزا و به مناسبت، انتخاب و استفاده میشوند. کارت A متشکل از 18 جزء ادراکی است. کارت B از 11 جزء هندسی تشکیل شده و مکمل کارت A است. در ابتدا از آزمودنی خواسته میشود به دلخواه تصویر یکی از کارتها را بکشد بعد از اتمام کار و پس از گذشت 3 دقیقه از او خواسته میشود دوباره تصویر را بکشد. مرحله نخست ترسیم به حساب توان رشد ترسیمی و ساختیابی ادراکی و مرحله دوم، با توجه به کمیت و کیفیت ترسیم مرحله نخست، سطح کارکرد حافظه دیداری را نشان خواهد داد. در کارت B مجموع نمرات کسبشده، 29 و در کارت A مجموع نمرات 36 است. کارت B برای ارزیابی ادراک و حافظه بینایی کودکان و کارت A برای بزرگسالان است. در این مطالعه نتایج کارت A تحلیل و بررسی شد. این آزمون را پناهی در سال 2005 در ایران اعتبارسنجی کرد و ضریب روایی آن حدود 50 و ضریب پایایی حدود 59 برآورد شده است [15].
پرسشنامه مربوط به اختلالات خواب پیتزبورگ
این پرسشنامه برای تعیین کیفیت خواب است که در اصل 9 گویه دارد، اما چون سؤال پنج خود شامل 10 گویه فرعی است، بنابراین کل پرسشنامه 19 آیتم دارد که از صفر تا 3 نمرهگذاری میشود. این پرسشنامه مؤلفههای مدت زمان خواب، کیفیت ذهنی خواب، تأخیر در بهخوابرفتن، میزان بازدهی خواب، اختلالات خواب، استفاده از داروهای خوابآور و اختلالات عملکردی روزانه را ارزیابی میکند. در این پرسشنامه کسب نمره کل بیشتر از 5 به معنی کیفیت خواب ضعیف است. شهریفر و حیدری این پرسشنامه را در سال 2011 در ایران اعتبارسنجی کردند و روایی 0/86 و پایایی 0/89 برای آن به دست آمد. ضریب الفای کرونباخ این پرسشنامه 0/78 تا 0/82 گزارش شده است [17 ،16].
یافتهها
نتایج بهدستآمده از بررسی 30 نمونه شرکتکننده در این پژوهش نشان داد جنسیت افراد، مساوی (50 درصد بیماران مذکر و 50 درصد مؤنث) و میانگین سنیشان 76/64 بود. همچنین بیش از 50 درصد افراد فشار خون بالا و بیش از 60 درصد اختلال خواب داشتند که وضعیت متغیرهای اصلی در جدول شماره 1 نشان داده شده است. تمام متغیرها بر اساس آزمون شاپیروویلکز توزیع نرمال داشتند (P>0/05). در جدول شماره 2 وضعیت شناختی (حافظه کلامی و بینایی) سالمندان نشان داده شده است که بیش از 96 درصد از سالمندان در حافظه بینایی و 70 درصد در حافظه کلامی اختلال داشتند. همچنین برای بررسی ارتباط بین متغیرهای حافظه کلامی و بینایی با اختلالات فشار خون و خواب از ضریب همبستگی اسپیرمن استفاده شد که در جدول شماره 3 بررسی شده است.
با توجه به جدول شماره 2، شرکتکنندگان نقایصی را در آزمون حافظه کلامی و بینایی داشتند. همچنین با توجه به جدول شماره 3، مشخص شد ارتباط معنیداری بین ابتلا به فشار خون بالا و اختلال خواب با حافظه بینایی، و ابتلا به فشار خون بالا با حافظه کلامی وجود دارد، اما ارتباط معنیداری بین ابتلا به اختلال خواب و حافظه کلامی پیدا نشد.
بحث
در سالمندی میزان شیوع انواع بیماریها افزایش مییابد (مثل بیماریهای قلبی یا بیماری آلزایمر)، اما هیچکدام از بیماریها، افزایش شیوع 400برابری ابتلا به پارکینسون را با افزایش سن نشان نمیدهد [4]. همچنین میزان ابتلا به اختلال فشار خون بالا و اختلالات خواب با افزایش سن، افزایش مییابد [19 ،18]. با افزایش سن، تغییراتی در کیفیت و ساختار خواب ایجاد میشود [18]. تحقیقات نشان داده است بعد از سردرد و اختلالات گوارشی، خواب با کیفیت ضعیف در رتبه سوم مشکلات سالمندان قرار دارد و از شکایات شایع و از دلایل مراجعه افراد سالمند به پزشکان است. تخمین زده میشود [20] بین 30 تا 45 درصد جمعیت دنیا به بیخوابی مبتلا هستند که با افزایش سن، میزان آن افزایش مییابد [21].
بحث
در سالمندی میزان شیوع انواع بیماریها افزایش مییابد (مثل بیماریهای قلبی یا بیماری آلزایمر)، اما هیچکدام از بیماریها، افزایش شیوع 400برابری ابتلا به پارکینسون را با افزایش سن نشان نمیدهد [4]. همچنین میزان ابتلا به اختلال فشار خون بالا و اختلالات خواب با افزایش سن، افزایش مییابد [19 ،18]. با افزایش سن، تغییراتی در کیفیت و ساختار خواب ایجاد میشود [18]. تحقیقات نشان داده است بعد از سردرد و اختلالات گوارشی، خواب با کیفیت ضعیف در رتبه سوم مشکلات سالمندان قرار دارد و از شکایات شایع و از دلایل مراجعه افراد سالمند به پزشکان است. تخمین زده میشود [20] بین 30 تا 45 درصد جمعیت دنیا به بیخوابی مبتلا هستند که با افزایش سن، میزان آن افزایش مییابد [21].
در این پژوهش نیز بیش از 50 درصد از شرکتکنندهها در این مطالعه، بر اساس خوداظهاری و بررسی تاریخچه پزشکی و داروهای مصرفی، فشار خون بالا داشتند. در حالی که مطالعه طوبی کاظمی و همکاران که در سال 2014 در ایران (بیرجند) برای بررسی شیوع فشار خون بالا روی 1286 فرد بزرگسال انجام شد، نشان داد حدود 20 درصد از جامعه موردبررسی فشار خون بالا داشتند [22]. این مسئله نشانگر شیوع بیشتر فشار خون بالا در سالمندان با اختلال پارکینسون در مقایسه با سالمندان عادی جامعه است. همچنین ارتباط معنیداری بین اختلال در فشار خون و بروز نواقص شناختی حافظه بینایی (P=0/031) و کلامی (P=0/004) یافت شد.
پس از جستوجوی پایگاههای دادهها، پژوهش زیادی درباره ارتباط بین ابتلا به فشار خون و نقایص شناختی در افراد با پارکینسون مشاهده نشد. فقط یک مطالعه در زمینه اختلالات فشار خون و نقایص شناختی یافت شد که نتایج این مطالعه با مطالعه سنت و همکاران (2016) که روی 18 نفر از سالمندان مبتلا به پارکینسون ایدیوپاتیک بدون دمانس مبتلا به فشار ارتواستاتیک و 19 نفر بدون اختلال فشار ارتواستاتیک انجام شده است، همسو بود. آنها بیان کردند افت فشار خون وضعیتی، در 53 درصد سالمندان مبتلا به پارکینسون مشاهده میشود و این افت فشار خون وضعیتی، میتواند روی شدت نقایص شناختی اثر بگذارد [9].
با توجه به مطالعه سیرا و همکاران که به بررسی آسیب رگهای کوچک و نواقص شناختی پرداختند، میتوان گفت فشار خون بالا باعث آسیب به عروق کوچک در نواحی مختلف مغز میشود که عارضه قابلمشاهدهای مثل سکته مغزی در افراد ایجاد نمیکند، اما با گذشت زمان باعث بروز نواقص شناختی میشود [23].
همچنین لادیکولا و همکاران در مطالعهای مروری که در سال 2017 برای بررسی ارتباط بین فشار خون بالا و ابتلا به نقایص شناختی انجام دادند، بیان کردند که فشار خون بالا میتواند باعث بروز اختلالاتی نظیر فشار خون بالا در ماده سفید مغز، خونریزیهای کوچک کورتیکالی و آتروفی مغز شود و احتمالاً روی عوامل شناختی (حافظه، توجه و عملکرد اجرایی) تأثیر بگذارد، اما نتایج قطعی هنوز مشخص نشده است [24].
با توجه به ماهیت بیماری پارکینسون در ایجاد اختلال بین سیستمهای استیل کولینی و دوپامینی که باعث نقص در عملکرد سیستم استیل کولین و برهمخوردن تعادل اعصاب سمپاتیک و تأثیر بر فشار خون میشود [25] و یافتههای این پژوهش دال بر شیوع فشار خون در سالمندان با پارکینسون، میتوان نتیجه گرفت فشار خون بالا میتواند عاملی برای تشدید نواقص شناختی در مبتلایان به پارکینسون شود.
از سوی دیگر، در این پژوهش بیش از 60 درصد شرکتکنندگان در این مطالعه، بر اساس خوداظهاری و تکمیل پرسشنامه اختلال خواب پیتزبورگ، اختلال خواب د اشتند، که این نتایج با مطالعات شین و همکاران که به بررسی ارتباط بین بیماری پارکینسون و اختلال خواب در جمعیت چین پرداختند، همسو بود [12]. آنان بیان کردند 48 تا 89 درصد سالمندان مبتلا به پارکینسون در کشور چین اختلال خواب دارند که بیشتر آنها از بیخوابی رنج میبرند [12]. همچنین مطالعه لکلیروویسونو و همکاران نشان داد بین اختلال خواب و ابتلا به اختلال شناختی در سالمندان مبتلا به پارکینسون ارتباط معنیداری وجود دارد؛ به نحوی که ابتلا به اختلال خواب و آپنه انسدادی خواب میتواند باعث بروز علائم غیرحرکتی در این افراد شود [11].
بنا به اظهارات شین و همکاران علت پاتوفیزیولوژی اختلال خواب در افراد مبتلا به پارکینسون به صورت قطعی مشخص نیست و میتواند به چند عامل بستگی داشته باشد که شامل اختلال در مرکز تنظیم خواب و بیداری، ظهور علائم حرکتی در شب، عوارض جانبی داروهای ضدپارکینسون، علائم روانپزشکی و منقطعشدن خواب است [12].
در مطالعه گردیسر و همکاران که در سال 2008 روی 143 نوجوان (میانگین سنی 14/9) با موضوع خواب نوجوانان و عملکرد حافظه فعال انجام گرفت، بیان شد هنگام خواب، پروجکشنهایی عمدتاً کولینرژیک بین هیپوکامپ و کورتکس اتفاق میافتد که تأثیر مستقیم بر عملکرد حافظه دارد و افرادی که کیفیت خواب ضعیفی دارند در زمینه حافظه ممکن است دچار مشکل شوند [26]. درنتیجه نقص حافظه در افراد مبتلا به پارکینسون میتواند با مشکلات خواب ارتباط مستقیم داشته باشد.
همچنین رولینسکی و همکاران در سال 2016 در مطالعه که روی اختلال حافظه کوتاهمدت بینایی و اختلال خواب حرکت سریع چشم در افراد مبتلا به پارکینسون انجام دادند، اظهار کردند کاهش فعالیت در بخش استریاتوم و ازدسترفتن نورونهای دوپامینرژیک باعث بروز اختلال خواب و نقص در حافظه کوتاهمدت بینایی میشود [27].
نتایج در این مطالعه نشان داد، بین اختلال خواب و اختلال در حافظه بینایی ارتباطی معنیدار وجود دارد که از عوامل مؤثر در اختلال حافظه بینایی است (P=0/045)، اما در زمینه حافظه کلامی ارتباط معناداری یافت نشد (P>0/05). بر اساس ارزیابیهای انجامشده در این پژوهش بنا بر اظهارات سالمندان و طبق ارزیابی اختلال خواب پیتزبورگ، بروز علائمی مانند بروز ترمور در یکسری از افراد هنگام خواب و فعالشدن اعصاب سمپاتیک و تکرر ادرار و منقطعشدن خواب در چندین مرحله در تمام افراد سالمند، از عوامل اصلی خواب ضعیف بود که خود میتواند بر عملکرد، استراحت مغز و برقراری ارتباطات بین هیپوکامپ و کورتکس تأثیر بگذارد و در پی آن منجر به بروز نواقص شناختی شود [26].
نتیجهگیری نهایی
نتایج این مطالعه نشان داد ارتباط معنیداری بین شاخصهای سلامت فرد و اختلالات حافظه وجود دارد. بنابراین، میتوان انتظار داشت با پیگیری این عوامل و کنترل آنها با مداخلات پزشکی بهنگام، بروز و شدت اختلالات شناختی در افراد سالمند مبتلا به پارکینسون تحت تأثیر قرار گیرد. از آنجایی که این پژوهش در شهر تهران انجام شده است و با توجه به متفاوتبودن سبک زندگی در شهرهای بزرگ، مانند تهران با سایر شهرستانها، توصیه میشود در بافتهای مختلف زندگی و همچنین بررسی نقش افراد خانواده، سبک زندگی و محل زندگی (شهرهای مدرن و صنعتی با بافت سنتی، تعداد بیشتر فرزندان و ارتباطات گستردهتر خانوادگی در سایر شهرها نسبت به تهران) پژوهشهایی انجام شود.
برای ارزیابی بهتر از وضعیت حافظه افراد سالمند با پارکینسون، پیشنهاد میشود اختلال در حافظه روالی با حافظه اخباری مقایسه شود.
ملاحظات اخلاقی
پیروی از اصول اخلاق پژوهش
این مقاله از دانشگاه علوم بهزیستی و توانبخشی کد اخلاقی (IR.USWR.REC.1396.105) دریافت کرده است. پس از کسب رضایت آگاهانه از شرکتکنندگان، فرایند جمعآوری اطلاعات آغاز شد.
حامی مالی
مقاله برگرفته از پایاننامه سیده مطهره حجازی در گروه کاردرمانی، دانشگاه علوم بهزیستی و توانبخشی، با عنوان ارتباط بین مشکلات شناختی با شاخص های سلامت در بیماران با پارکینسون است و تحت حمایت مالی واحد توسعه تحقیقات بالینی بیمارستان توانبخشی رفیده بوده است.
مشارکت نویسندگان
مفهوم سازی: سیده مطهره حجازی، نازیلا اکبر فهیمی، حجت اله حقگو؛ روش شناسی:سیده مطهره حجازی، نازیلا اکبر فهیمی، حجت اله حقگو، اشرف کربلایی نوری؛ تحلیل و تحقیق: اکبر بیگلریان و سیده مطهره حجازی و نازیلا اکبرفهیمی؛ نگارش پیش نویس: سیده مطهره حجازی، نازیلا اکبر فهیمی، حجت اله حقگو؛ ویراستاری نهایی: حجت اله حقگو و نازیلا اکبرفهیمی
تعارض منافع
بنا به اظهار نویسندگان، در این مقاله هیچگونه تعارض منافعی وجود ندارد.
تشکر و قدردانی
از تمامی سالمندان گرامی شرکتکننده در این مطالعه، همراهان شرکتکنندهها، ریاست و کارکنان محترم بیمارستان توانبخشی رفیده که محققان را برای انجام این پژوهش یاری کردند، کمال تشکر را داریم.
پس از جستوجوی پایگاههای دادهها، پژوهش زیادی درباره ارتباط بین ابتلا به فشار خون و نقایص شناختی در افراد با پارکینسون مشاهده نشد. فقط یک مطالعه در زمینه اختلالات فشار خون و نقایص شناختی یافت شد که نتایج این مطالعه با مطالعه سنت و همکاران (2016) که روی 18 نفر از سالمندان مبتلا به پارکینسون ایدیوپاتیک بدون دمانس مبتلا به فشار ارتواستاتیک و 19 نفر بدون اختلال فشار ارتواستاتیک انجام شده است، همسو بود. آنها بیان کردند افت فشار خون وضعیتی، در 53 درصد سالمندان مبتلا به پارکینسون مشاهده میشود و این افت فشار خون وضعیتی، میتواند روی شدت نقایص شناختی اثر بگذارد [9].
با توجه به مطالعه سیرا و همکاران که به بررسی آسیب رگهای کوچک و نواقص شناختی پرداختند، میتوان گفت فشار خون بالا باعث آسیب به عروق کوچک در نواحی مختلف مغز میشود که عارضه قابلمشاهدهای مثل سکته مغزی در افراد ایجاد نمیکند، اما با گذشت زمان باعث بروز نواقص شناختی میشود [23].
همچنین لادیکولا و همکاران در مطالعهای مروری که در سال 2017 برای بررسی ارتباط بین فشار خون بالا و ابتلا به نقایص شناختی انجام دادند، بیان کردند که فشار خون بالا میتواند باعث بروز اختلالاتی نظیر فشار خون بالا در ماده سفید مغز، خونریزیهای کوچک کورتیکالی و آتروفی مغز شود و احتمالاً روی عوامل شناختی (حافظه، توجه و عملکرد اجرایی) تأثیر بگذارد، اما نتایج قطعی هنوز مشخص نشده است [24].
با توجه به ماهیت بیماری پارکینسون در ایجاد اختلال بین سیستمهای استیل کولینی و دوپامینی که باعث نقص در عملکرد سیستم استیل کولین و برهمخوردن تعادل اعصاب سمپاتیک و تأثیر بر فشار خون میشود [25] و یافتههای این پژوهش دال بر شیوع فشار خون در سالمندان با پارکینسون، میتوان نتیجه گرفت فشار خون بالا میتواند عاملی برای تشدید نواقص شناختی در مبتلایان به پارکینسون شود.
از سوی دیگر، در این پژوهش بیش از 60 درصد شرکتکنندگان در این مطالعه، بر اساس خوداظهاری و تکمیل پرسشنامه اختلال خواب پیتزبورگ، اختلال خواب د اشتند، که این نتایج با مطالعات شین و همکاران که به بررسی ارتباط بین بیماری پارکینسون و اختلال خواب در جمعیت چین پرداختند، همسو بود [12]. آنان بیان کردند 48 تا 89 درصد سالمندان مبتلا به پارکینسون در کشور چین اختلال خواب دارند که بیشتر آنها از بیخوابی رنج میبرند [12]. همچنین مطالعه لکلیروویسونو و همکاران نشان داد بین اختلال خواب و ابتلا به اختلال شناختی در سالمندان مبتلا به پارکینسون ارتباط معنیداری وجود دارد؛ به نحوی که ابتلا به اختلال خواب و آپنه انسدادی خواب میتواند باعث بروز علائم غیرحرکتی در این افراد شود [11].
بنا به اظهارات شین و همکاران علت پاتوفیزیولوژی اختلال خواب در افراد مبتلا به پارکینسون به صورت قطعی مشخص نیست و میتواند به چند عامل بستگی داشته باشد که شامل اختلال در مرکز تنظیم خواب و بیداری، ظهور علائم حرکتی در شب، عوارض جانبی داروهای ضدپارکینسون، علائم روانپزشکی و منقطعشدن خواب است [12].
در مطالعه گردیسر و همکاران که در سال 2008 روی 143 نوجوان (میانگین سنی 14/9) با موضوع خواب نوجوانان و عملکرد حافظه فعال انجام گرفت، بیان شد هنگام خواب، پروجکشنهایی عمدتاً کولینرژیک بین هیپوکامپ و کورتکس اتفاق میافتد که تأثیر مستقیم بر عملکرد حافظه دارد و افرادی که کیفیت خواب ضعیفی دارند در زمینه حافظه ممکن است دچار مشکل شوند [26]. درنتیجه نقص حافظه در افراد مبتلا به پارکینسون میتواند با مشکلات خواب ارتباط مستقیم داشته باشد.
همچنین رولینسکی و همکاران در سال 2016 در مطالعه که روی اختلال حافظه کوتاهمدت بینایی و اختلال خواب حرکت سریع چشم در افراد مبتلا به پارکینسون انجام دادند، اظهار کردند کاهش فعالیت در بخش استریاتوم و ازدسترفتن نورونهای دوپامینرژیک باعث بروز اختلال خواب و نقص در حافظه کوتاهمدت بینایی میشود [27].
نتایج در این مطالعه نشان داد، بین اختلال خواب و اختلال در حافظه بینایی ارتباطی معنیدار وجود دارد که از عوامل مؤثر در اختلال حافظه بینایی است (P=0/045)، اما در زمینه حافظه کلامی ارتباط معناداری یافت نشد (P>0/05). بر اساس ارزیابیهای انجامشده در این پژوهش بنا بر اظهارات سالمندان و طبق ارزیابی اختلال خواب پیتزبورگ، بروز علائمی مانند بروز ترمور در یکسری از افراد هنگام خواب و فعالشدن اعصاب سمپاتیک و تکرر ادرار و منقطعشدن خواب در چندین مرحله در تمام افراد سالمند، از عوامل اصلی خواب ضعیف بود که خود میتواند بر عملکرد، استراحت مغز و برقراری ارتباطات بین هیپوکامپ و کورتکس تأثیر بگذارد و در پی آن منجر به بروز نواقص شناختی شود [26].
نتیجهگیری نهایی
نتایج این مطالعه نشان داد ارتباط معنیداری بین شاخصهای سلامت فرد و اختلالات حافظه وجود دارد. بنابراین، میتوان انتظار داشت با پیگیری این عوامل و کنترل آنها با مداخلات پزشکی بهنگام، بروز و شدت اختلالات شناختی در افراد سالمند مبتلا به پارکینسون تحت تأثیر قرار گیرد. از آنجایی که این پژوهش در شهر تهران انجام شده است و با توجه به متفاوتبودن سبک زندگی در شهرهای بزرگ، مانند تهران با سایر شهرستانها، توصیه میشود در بافتهای مختلف زندگی و همچنین بررسی نقش افراد خانواده، سبک زندگی و محل زندگی (شهرهای مدرن و صنعتی با بافت سنتی، تعداد بیشتر فرزندان و ارتباطات گستردهتر خانوادگی در سایر شهرها نسبت به تهران) پژوهشهایی انجام شود.
برای ارزیابی بهتر از وضعیت حافظه افراد سالمند با پارکینسون، پیشنهاد میشود اختلال در حافظه روالی با حافظه اخباری مقایسه شود.
ملاحظات اخلاقی
پیروی از اصول اخلاق پژوهش
این مقاله از دانشگاه علوم بهزیستی و توانبخشی کد اخلاقی (IR.USWR.REC.1396.105) دریافت کرده است. پس از کسب رضایت آگاهانه از شرکتکنندگان، فرایند جمعآوری اطلاعات آغاز شد.
حامی مالی
مقاله برگرفته از پایاننامه سیده مطهره حجازی در گروه کاردرمانی، دانشگاه علوم بهزیستی و توانبخشی، با عنوان ارتباط بین مشکلات شناختی با شاخص های سلامت در بیماران با پارکینسون است و تحت حمایت مالی واحد توسعه تحقیقات بالینی بیمارستان توانبخشی رفیده بوده است.
مشارکت نویسندگان
مفهوم سازی: سیده مطهره حجازی، نازیلا اکبر فهیمی، حجت اله حقگو؛ روش شناسی:سیده مطهره حجازی، نازیلا اکبر فهیمی، حجت اله حقگو، اشرف کربلایی نوری؛ تحلیل و تحقیق: اکبر بیگلریان و سیده مطهره حجازی و نازیلا اکبرفهیمی؛ نگارش پیش نویس: سیده مطهره حجازی، نازیلا اکبر فهیمی، حجت اله حقگو؛ ویراستاری نهایی: حجت اله حقگو و نازیلا اکبرفهیمی
تعارض منافع
بنا به اظهار نویسندگان، در این مقاله هیچگونه تعارض منافعی وجود ندارد.
تشکر و قدردانی
از تمامی سالمندان گرامی شرکتکننده در این مطالعه، همراهان شرکتکنندهها، ریاست و کارکنان محترم بیمارستان توانبخشی رفیده که محققان را برای انجام این پژوهش یاری کردند، کمال تشکر را داریم.
References
World Health Organization. World Health Statistics 2012. Geneva: World Health Organization; 2012.
Habibi A, Nikpour S, Seyedoshohadaei M, Haghani H. [Health promoting behaviors and its related factors in elderly (Persian)]. Iran Journal of Nursing. 2006; 19(47):35-48.
Kalia LV, Kalia SK, Lang AE. Disease‐modifying strategies for Parkinson’s disease. Movement Disorders. 2015; 30(11):1442-50. [DOI:10.1002/mds.26354] [PMID]
Rodriguez M, Rodriguez Sabate C, Morales I, Sanchez A, Sabate M. Parkinson’s disease as a result of aging. Aging Cell. 2015; 14(3):293-308. [DOI:10.1111/acel.12312] [PMID] [PMCID]
Goetz CG. The history of Parkinson’s disease: Early clinical descriptions and neurological therapies. Cold Spring Harbor Perspectives in Medicine. 2011; 1(1):a008862. [DOI:10.1101/cshperspect.a008862] [PMID] [PMCID]
Litvan I, Aarsland D, Adler CH, Goldman JG, Kulisevsky J, Mollenhauer B, et al. MDS task force on mild cognitive impairment in Parkinson’s disease: Critical review of PD‐MCI. Movement Disorders. 2011; 26(10):1814-24. [DOI:10.1002/mds.23823] [PMID] [PMCID]
Azuma T, Cruz RF, Bayles KA, Tomoeda CK, Montgomery EB. A longitudinal study of neuropsychological change in individuals with Parkinson’s disease. International Journal of Geriatric Psychiatry. 2003; 18(12):1115-20. [DOI:10.1002/gps.1022] [PMID]
Petersen RC. Mild cognitive impairment as a diagnostic entity. Journal of Internal Medicine. 2004; 256(3):183-94. [DOI:10.1111/j.1365-2796.2004.01388.x] [PMID]
Centi J, Freeman R, Gibbons CH, Neargarder S, Canova AO, Cronin Golomb A. Effects of orthostatic hypotension on cognition in Parkinson disease. Neurology. 2017; 88(1):17-24. [DOI:10.1212/WNL.0000000000003452]
Chahine LM, Weintraub D, Hawkins KA, Siderowf A, Eberly S, Oakes D, et al. Cognition in individuals at risk for Parkinson’s: Parkinson Associated Risk Syndrome (PARS) study findings. Movement Disorders. 2016; 31(1):86-94. [DOI:10.1002/mds.26373] [PMID] [PMCID]
Leclair Visonneau L, Clairembault T, Coron E, Le Dily S, Vavasseur F, Dalichampt M, et al. REM sleep behavior disorder is related to enteric neuropathology in Parkinson disease. Neurology. 2017; 89(15):1612-8. [DOI:10.1212/WNL.0000000000004496] [PMID]
Shen Y, Liu CF. Sleep disorders in Parkinson’s disease: Present status and future prospects. Chinese Medical Journal. 2018; 131(8):883-5. [DOI:10.4103/0366-6999.229903] [PMID] [PMCID]
Emsaki G, Molavi H, Chitsaz A, Abtahi MM, Asgari K. [Psychometric properties of the Montreal Cognitive Assessment (MoCA) in Parkinson’s disease patients in Isfahan (Persian)]. Journal of Isfahan Medical School. 2011; 29(158):1391-400.
Saed O, Rushan R, Moradi A. [Investigating psychometric properties of Wechsler Memory Scale-for the students of Tehran Universities (Persian)]. Clinical Psychology & Personality. 2008; 1(31):57-70.
Nazaribadie M, Asgari K, Amini M, Abedi A. [An investigation of the cognitive performances in patients with type 2 diabetes in comparison to pre-diabetic patients (Persian)]. Advances in Cognitive Science. 2011; 13(3):33-40.
Buysse DJ, Reynolds CF, Monk TH, Berman SR, Kupfer DJ. The Pittsburgh Sleep Quality Index: A new instrument for psychiatric practice and research. Psychiatry Research. 1989; 28(2):193-213. [DOI:10.1016/0165-1781(89)90047-4]
Heidari A, Ehteshamzadeh P, Marashi M. [The relationship between insomnia intensity, sleep quality, sleepiness and mental health disorder with educational performance in female adolescences of Ahwaz city (Persian)]. Woman and Culture. 2010; 1(4):65-76.
Reid KJ, Martinovich Z, Finkel S, Statsinger J, Golden R, Harter K, et al. Sleep: A marker of physical and mental health in the elderly. The American Journal of Geriatric Psychiatry. 2006; 14(10):860-6. [DOI:10.1097/01.JGP.0000206164.56404.ba] [PMID]
Ahangari M, Kamali M, Arjmand hesabi M. [The effects of high blood pressure on the quality of life of the elderly in the elderly cultural center of Tehran (Persian)]. Iranian Journal of Aging. 2008; 3(7):26-32.
Cotroneo A, Gareri P, Lacava R, Cabodi S. Use of zolpidem in over 75-year-old patients with sleep disorders and comorbidities. Archives of Gerontology and Geriatrics Supplement. 2004; (9):93-6. [DOI:10.1016/j.archger.2004.04.015] [PMID]
Leger D, Poursain B, Neubauer D, Uchiyama M. An international survey of sleeping problems in the general population. Current Medical Research and Opinion. 2008; 24(1):307-17. [DOI:10.1185/030079907X253771] [PMID]
Kazemi T, Hajihosseini M, Mashreghimoghadam H, Azdaki N, Ziaee M. Prevalence and determinants of hypertension among Iranian adults, Birjand, Iran. International Journal of Preventive Medicine. 2017; 8:36.
Sierra C. Cerebral small vessel disease, cognitive impairment and vascular dementia. Panminerva Medica. 2012; 54(3):179-88. [PMID]
Iadecola C, Yaffe K, Biller J, Bratzke LC, Faraci FM, Gorelick PB, et al. Impact of hypertension on cognitive function: A scientific statement from the American Heart Association. Hypertension. 2016; 68(6):e67-e94. [DOI:10.1161/HYP.0000000000000053] [PMID] [PMCID]
Rizzi G. Dopamine and acetylcholine, a circuit point of view in Parkinson’s disease. Frontiers in Neural Circuits. 2017; 11:110. [DOI:10.3389/fncir.2017.00110] [PMID] [PMCID]
Gradisar M, Terrill G, Johnston A, Douglas P. Adolescent sleep and working memory performance. Sleep and Biological Rhythms. 2008; 6(3):146-54. [DOI:10.1111/j.1479-8425.2008.00353.x]
Rolinski M, Zokaei N, Baig F, Giehl K, Quinnell T, Zaiwalla Z, et al. Visual short-term memory deficits in REM sleep behaviour disorder mirror those in Parkinson’s disease. Brain. 2015; 139(1):47-53. [DOI:10.1093/brain/awv334] [PMID] [PMCID]
World Health Organization. World Health Statistics 2012. Geneva: World Health Organization; 2012.
Habibi A, Nikpour S, Seyedoshohadaei M, Haghani H. [Health promoting behaviors and its related factors in elderly (Persian)]. Iran Journal of Nursing. 2006; 19(47):35-48.
Kalia LV, Kalia SK, Lang AE. Disease‐modifying strategies for Parkinson’s disease. Movement Disorders. 2015; 30(11):1442-50. [DOI:10.1002/mds.26354] [PMID]
Rodriguez M, Rodriguez Sabate C, Morales I, Sanchez A, Sabate M. Parkinson’s disease as a result of aging. Aging Cell. 2015; 14(3):293-308. [DOI:10.1111/acel.12312] [PMID] [PMCID]
Goetz CG. The history of Parkinson’s disease: Early clinical descriptions and neurological therapies. Cold Spring Harbor Perspectives in Medicine. 2011; 1(1):a008862. [DOI:10.1101/cshperspect.a008862] [PMID] [PMCID]
Litvan I, Aarsland D, Adler CH, Goldman JG, Kulisevsky J, Mollenhauer B, et al. MDS task force on mild cognitive impairment in Parkinson’s disease: Critical review of PD‐MCI. Movement Disorders. 2011; 26(10):1814-24. [DOI:10.1002/mds.23823] [PMID] [PMCID]
Azuma T, Cruz RF, Bayles KA, Tomoeda CK, Montgomery EB. A longitudinal study of neuropsychological change in individuals with Parkinson’s disease. International Journal of Geriatric Psychiatry. 2003; 18(12):1115-20. [DOI:10.1002/gps.1022] [PMID]
Petersen RC. Mild cognitive impairment as a diagnostic entity. Journal of Internal Medicine. 2004; 256(3):183-94. [DOI:10.1111/j.1365-2796.2004.01388.x] [PMID]
Centi J, Freeman R, Gibbons CH, Neargarder S, Canova AO, Cronin Golomb A. Effects of orthostatic hypotension on cognition in Parkinson disease. Neurology. 2017; 88(1):17-24. [DOI:10.1212/WNL.0000000000003452]
Chahine LM, Weintraub D, Hawkins KA, Siderowf A, Eberly S, Oakes D, et al. Cognition in individuals at risk for Parkinson’s: Parkinson Associated Risk Syndrome (PARS) study findings. Movement Disorders. 2016; 31(1):86-94. [DOI:10.1002/mds.26373] [PMID] [PMCID]
Leclair Visonneau L, Clairembault T, Coron E, Le Dily S, Vavasseur F, Dalichampt M, et al. REM sleep behavior disorder is related to enteric neuropathology in Parkinson disease. Neurology. 2017; 89(15):1612-8. [DOI:10.1212/WNL.0000000000004496] [PMID]
Shen Y, Liu CF. Sleep disorders in Parkinson’s disease: Present status and future prospects. Chinese Medical Journal. 2018; 131(8):883-5. [DOI:10.4103/0366-6999.229903] [PMID] [PMCID]
Emsaki G, Molavi H, Chitsaz A, Abtahi MM, Asgari K. [Psychometric properties of the Montreal Cognitive Assessment (MoCA) in Parkinson’s disease patients in Isfahan (Persian)]. Journal of Isfahan Medical School. 2011; 29(158):1391-400.
Saed O, Rushan R, Moradi A. [Investigating psychometric properties of Wechsler Memory Scale-for the students of Tehran Universities (Persian)]. Clinical Psychology & Personality. 2008; 1(31):57-70.
Nazaribadie M, Asgari K, Amini M, Abedi A. [An investigation of the cognitive performances in patients with type 2 diabetes in comparison to pre-diabetic patients (Persian)]. Advances in Cognitive Science. 2011; 13(3):33-40.
Buysse DJ, Reynolds CF, Monk TH, Berman SR, Kupfer DJ. The Pittsburgh Sleep Quality Index: A new instrument for psychiatric practice and research. Psychiatry Research. 1989; 28(2):193-213. [DOI:10.1016/0165-1781(89)90047-4]
Heidari A, Ehteshamzadeh P, Marashi M. [The relationship between insomnia intensity, sleep quality, sleepiness and mental health disorder with educational performance in female adolescences of Ahwaz city (Persian)]. Woman and Culture. 2010; 1(4):65-76.
Reid KJ, Martinovich Z, Finkel S, Statsinger J, Golden R, Harter K, et al. Sleep: A marker of physical and mental health in the elderly. The American Journal of Geriatric Psychiatry. 2006; 14(10):860-6. [DOI:10.1097/01.JGP.0000206164.56404.ba] [PMID]
Ahangari M, Kamali M, Arjmand hesabi M. [The effects of high blood pressure on the quality of life of the elderly in the elderly cultural center of Tehran (Persian)]. Iranian Journal of Aging. 2008; 3(7):26-32.
Cotroneo A, Gareri P, Lacava R, Cabodi S. Use of zolpidem in over 75-year-old patients with sleep disorders and comorbidities. Archives of Gerontology and Geriatrics Supplement. 2004; (9):93-6. [DOI:10.1016/j.archger.2004.04.015] [PMID]
Leger D, Poursain B, Neubauer D, Uchiyama M. An international survey of sleeping problems in the general population. Current Medical Research and Opinion. 2008; 24(1):307-17. [DOI:10.1185/030079907X253771] [PMID]
Kazemi T, Hajihosseini M, Mashreghimoghadam H, Azdaki N, Ziaee M. Prevalence and determinants of hypertension among Iranian adults, Birjand, Iran. International Journal of Preventive Medicine. 2017; 8:36.
Sierra C. Cerebral small vessel disease, cognitive impairment and vascular dementia. Panminerva Medica. 2012; 54(3):179-88. [PMID]
Iadecola C, Yaffe K, Biller J, Bratzke LC, Faraci FM, Gorelick PB, et al. Impact of hypertension on cognitive function: A scientific statement from the American Heart Association. Hypertension. 2016; 68(6):e67-e94. [DOI:10.1161/HYP.0000000000000053] [PMID] [PMCID]
Rizzi G. Dopamine and acetylcholine, a circuit point of view in Parkinson’s disease. Frontiers in Neural Circuits. 2017; 11:110. [DOI:10.3389/fncir.2017.00110] [PMID] [PMCID]
Gradisar M, Terrill G, Johnston A, Douglas P. Adolescent sleep and working memory performance. Sleep and Biological Rhythms. 2008; 6(3):146-54. [DOI:10.1111/j.1479-8425.2008.00353.x]
Rolinski M, Zokaei N, Baig F, Giehl K, Quinnell T, Zaiwalla Z, et al. Visual short-term memory deficits in REM sleep behaviour disorder mirror those in Parkinson’s disease. Brain. 2015; 139(1):47-53. [DOI:10.1093/brain/awv334] [PMID] [PMCID]
نوع مطالعه: پژوهشي |
موضوع مقاله:
سالمند شناسی
دریافت: 1397/6/1 | پذیرش: 1397/10/19 | انتشار: 1397/12/19
دریافت: 1397/6/1 | پذیرش: 1397/10/19 | انتشار: 1397/12/19
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |